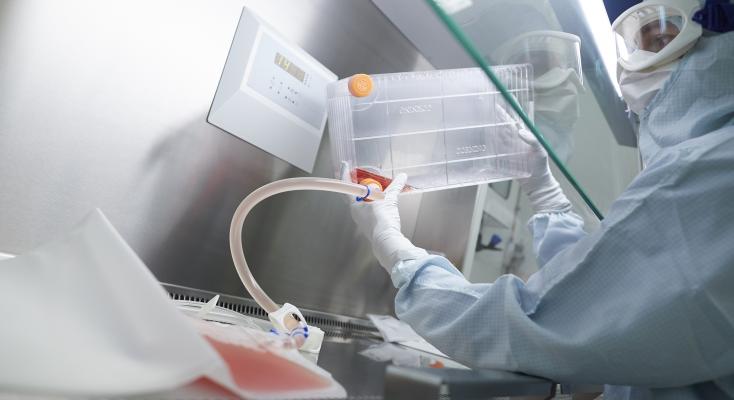
Thérapie cellulaire
Atlantic Bio GMP assure la production de Médicaments de Thérapie Innovante dans le cadre d’essais cliniques en Thérapie Cellulaire dans les domaines de la médecine régénérative (Cellules Souches Mésenchymateuse, hESC…) et de l’immunothérapie (CART-Cells, CTL…).
Atlantic Bio GMP propose différentes prestations en thérapie cellulaire, tout au long du projet :
- Production de lots pilotes, lots de développement, lots de validation,
- Production de banques,
- Production de lots cliniques,
- Contrôle qualité, études de stabilité,
- Stockage sécurisé,
- Accompagnement.
Exemples de prestations en thérapie cellulaire
Prestation dans la cadre du protocole EXCELLENT en partenariat avec CellProthera
Pathologie traitée : infarctus du myocarde
Mission d’Atlantic Bio GMP : Expansion de CD34+, production de lots cliniques pour un essai de phase II mené à Bordeaux, Grenoble, Massy, Montpellier et Toulouse (France)
Le concept thérapeutique unique développé par Cell Prothera consiste à régénérer les tissus cardiaques endommagés lors de l’infarctus grâce à l’injection de cellules souches du patient directement dans la zone lésée.
Atlantic Bio GMP reçoit les cellules souches prélevées sur le patient et réalise leur expansion pour fabriquer le greffon qui sera injecté dans le muscle cardiaque. Cette thérapie autologue, mini-invasive, à terme administrée en ambulatoire, pourrait devenir une alternative à la transplantation cardiaque et permettre d’éviter l’insuffisance cardiaque liée à l’infarctus du myocarde.
Pour en savoir plus : www.cellprothera.com
Collaboration dans le cadre de l'étude MESAMI en partenariat avec le CHU de Toulouse
Pathologie traitée : insuffisance cardiaque chronique
Mission d’Atlantic Bio GMP : CSM, production de lots cliniques et de placebos pour un essai de phase II en double aveugle randomisé mené à Bordeaux, Créteil, Montpellier et Toulouse (France)
En cas d’insuffisance cardiaque chronique, les CSM peuvent stimuler les capacités de réparation du muscle cardiaque en revascularisant les zones lésées. L’essai MESAMI d’une équipe du CHU de Toulouse a pour but d’injecter des CSM issues de la moelle osseuse du patient dans les zones saines de son cœur en passant par l’artère fémorale. Dans le cadre de la phase II de l’essai clinique, Atlantic Bio GMP reçoit, met en culture puis libère les CSM qui seront injectées au patient et produit les placebos.
Prestation dans le cadre du programme STREAM, CECS en partenariat avec I-Stem
Pathologies traitées : rétinite pigmentaire
Mission d’Atlantic Bio GMP : Banque RPE et cellules RPE dérivées de HESC, production d’une matière première de départ cellulaire (banque) puis des unités thérapeutiques pour un essai clinique de phase I
Les pathologies rétiniennes dégénératives (dont la rétinite pigmentaire) sont les causes principales de la cécité chez l’homme et sont très difficiles à traiter. I-Stem se base sur le caractère pluripotentiel des hESC et sur leur capacité à se différencier pour tenter de développer des traitements de thérapie cellulaire permettant de traiter un large spectre de rétinopathies. Les premiers travaux d’I-Stem ont démontré que les hESC sont une source de progéniteurs rétiniens utilisables en thérapie cellulaire. Atlantic Bio GMP produit donc des cellules RPE dérivées de hESC (dans un premier temps une banque, puis des unités thérapeutiques) pour un essai clinique de phase I prévu en 2018.
Pour en savoir plus www.istem.eu